[Rodent Whole Body Perfusion이란?]
고정의 목표는 조직을 살아있을 때와 유사한 상태로 빠르고 균일하게 보존하는 것입니다. 작은 조직은 고정액에 직접 담그는 방법이 효과적이지만, 뇌와 같은 큰 표본은 고정액이 모든 부위에 동일한 속도로 도달하지 않아 침지 고정이 어렵습니다. 순환계를 통해 고정액을 직접 주입하면 혈관 네트워크를 통해 신속하게 조직 전체에 고정액이 퍼질 수 있다는 장점이 있습니다.
Whole body perfusion은 심장의 대동맥에서 가깝게 공급되는 혈액으로 순환되는 ‘뇌’와 같은 장기들을 고정할 때 적합합니다. 관류의 최종 성공 지표는 조직의 초미세구조의 보존입니다.
[Rodent Whole Body Perfusion 준비]
1. 관류 장치
Whole body perfusion을 위해서 순환계를 효과적으로 활용하려면 생리적 압력에 맞춰 일정한 압력을 유지하며 고정액을 관류하는 것이 중요합니다. 이를 위해 적절한 관류 장치가 필요할 수 있습니다.
2. Fixative & Perfusion Buffers
1) Fixative: 4% Paraformaldehyde Fixative (Fixative 8% Paraformaldehyde Stock + 0.2M Sodium Phosphate Buffer; pH 7.4)
2) Perfusion Buffers
- Phosphate Buffered Saline; pH 7.4
- HEPES Buffered Hanks Solution(HBHS) with Sodium Azide; pH 7.4
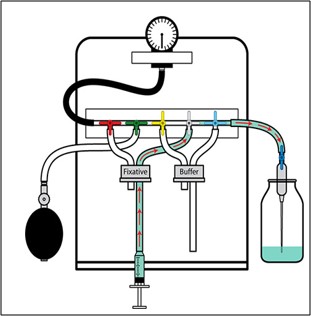
그림 1. 관류장치 예시
* 참고 동영상: Gage GJ et al. J Vis Exp. 2012;(65):3564.
[Rodent Whole Body Perfusion 과정]
1. 관류 장치 준비
1) 고정액 라인 준비
먼저 고정액 라인을 준비합니다. 주사기를 사용하여 버퍼를 빠르게 주입하고 빼내면서 튜브 내 공기 방울을 제거하고 버퍼로 채웁니다. 그 다음, 바늘 끝의 밸브를 닫습니다. 고정액 라인을 고정액 병에 연결할 때 공기 방울이 들어가지 않도록 주의하십시오.
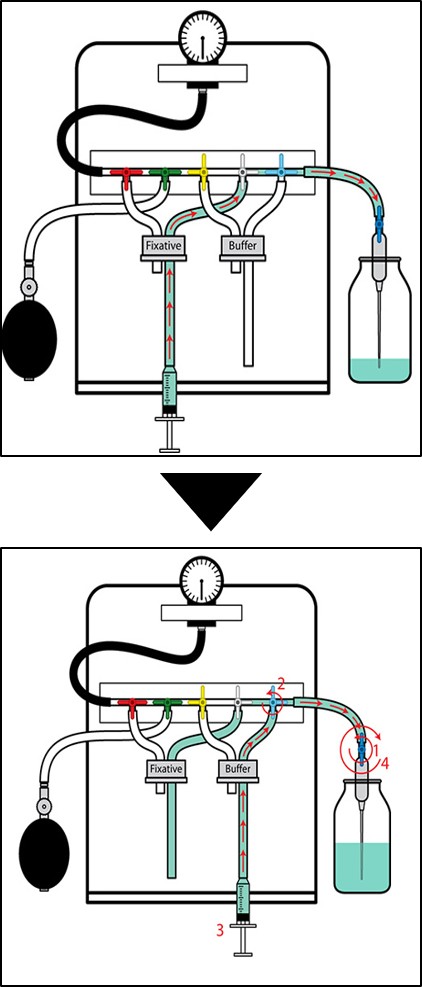
그림 2. 관류장치 준비
2) 버퍼 라인 준비
먼저 바늘 끝의 밸브를 열고 버퍼 밸브(파란색)를 흐름 위치로 돌립니다. 주사기를 사용하여 버퍼를 빠르게 주입하고 빼내면서 튜뷰 내 공기 방울을 제거하고 버퍼로 채운 후, 바늘 끝의 밸브를 닫습니다. 튜브를 버퍼 병에 연결하고, 마노미터 블러브를 펌핑하여 압력을 테스트하고 게이지를 확인하여 시스템이 제대로 밀봉되었는지 확인합니다.
2. 관류 수술
1) 동물이 수술에 적합한 마취 상태에 도달하면, 으깬 얼음으로 채운 얕은 트레이에 동물을 올려놓습니다.
2) 피부와 복벽을 가로로 절개한 후, 횡격막에 절개를 가하고 횡격막을 가로로 잘라 심장을 노출시킵니다. 늑골을 따라 평행하게 절개를 진행하여 쇄골까지 자릅니다. 이후 흉골 끝을 지혈기로 잡고 지혈기를 머리 쪽으로 이동시킵니다.
3) 관류 바늘을 좌심실을 통해 상행 대동맥에 삽입한 후, 지혈기를 사용하여 심장을 고정하고 바늘이 움직이지 않도록 합니다. 바늘 끝 주변의 대동맥을 고정하기 위해 수정된 지혈기를 추가로 사용할 수 있습니다. 이후 홍채 가위를 사용하여 좌심실의 후방 끝에 작은 절개를 가합니다.
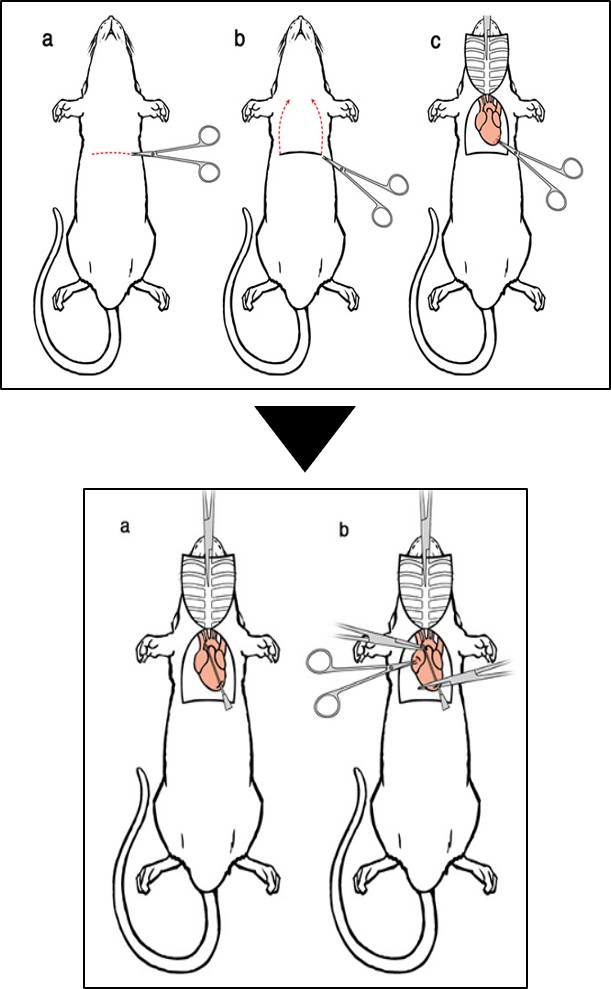
그림 3. 관류수술 1
4) 배출 포트를 열고 바늘 베이스에 연결하면서 공기 방울이 들어가지 않도록 주의합니다.
5) 마노미터 블러브를 80mmHg의 압력으로 신속하고 균일하게 펌핑합니다. 이 압력을 버퍼 주입 동안 유지해야 하며 관류 시간을 측정하기 위한 타이머를 시작합니다.
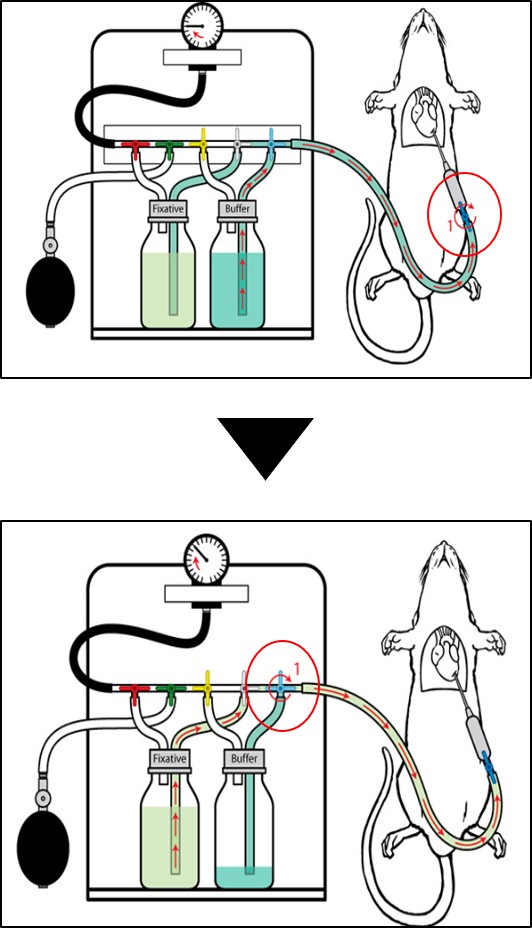
그림 4. 관류수술 2
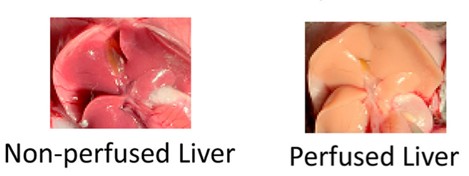
6) 버퍼가 거의 소진되면(200ml) 버퍼 밸브(파란색)를 전환합니다. 이 때, 액체가 맑게 흐르고 있어야 합니다. 간이 맑아지는 것은 관류가 잘 이루어지고 있다는 신호이며 이 시점에서 간이 맑아져야 합니다.
7) 압력은 최대 130 mmHg까지 점진적으로 증가시켜 안정적인 유속을 유지할 수 있으며 고정액이 소진되면 배출 밸브를 닫고 종료 시간을 기록합니다.
3. 관류 확인
관류의 성공 여부를 초기적으로 판단할 수 있는 지표는 코, 귀, 발과 같은 외부 사지와 흉선 및 간과 같은 내부 장기의 혈액이 제거되는 것입니다. 뇌의 육안 검사를 통해 혈관이 혈액이 없어 흰색에서 연한 노란색으로 변하며 조직 절편에서도 마찬가지로 확인될 수 있습니다.
* 그림출처: Gage GJ et al. J Vis Exp. 2012;(65):3564.