* 제브라피쉬 운동신경계
제브라피쉬(zebrafish, Danio rerio)는 운동신경계는 구조적으로 단순하면서도 보존성이 높아,
포유류 운동신경계의 기본 원리를 잘 반영하고 있어 척추동물 신경계 연구, 특히 운동신경계 발달과 기능을 이해하는 데 널리 쓰이고 있습니다.
인간의 운동 신경계는 척수 (spinal cord), 뇌간 (brainstem), 운동피질 (motor cortex)의 세 가지 제어 수준으로 계층적으로 구성되어 있으나, 제브라피쉬의 운동신경계는 대뇌운동피질 경로가 없으며, 뇌간에서 운동명령을 전달하는 상위 신경세포와 하위의 근육과 연결된 신경회로를 가집니다.
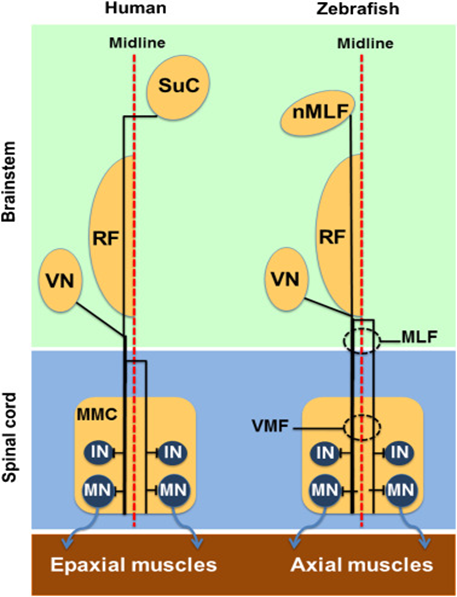
* 그림 출처: Prog Neurobiol. 2014 Jul;118:36-58.
◆ 1차 운동신경세포 (Primary motor neuron, PMNs)
- 배아기 (약 수정 후 17-20시간)부터 가장 먼저 발생됨
- 큰 세포체와 축삭을 가지며, 수가 적음
- fast muscle 에 운동신경(motor nerve)이 연결됨
- 크고 빠른 반응과 강한 수축성 운동을 조절
(escape, fast swimming, spontaneous coiling)
- 운동신경세포의 축삭 방향에 따라 4가지 유형으로 구분
• CaP (Caudal Primary motor neuron): 척수에서 배측으로 나와 꼬리근육 ventral 영역을 조절.
• MiP (Middle Primary motor neuron): 등쪽으로 뻗어 dorsal 근육을 조절.
• RoP (Rostral Primary motor neuron): 상대적으로 작은 세포, 주로 몸통 근육 innervation.
• VaP (Variable Primary motor neuron): 일부 개체에서만 나타남.
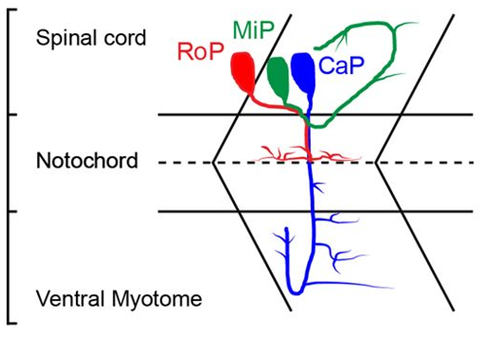
* 그림 출처: Dis Model Mech (2012) 5 (6): 921–929.
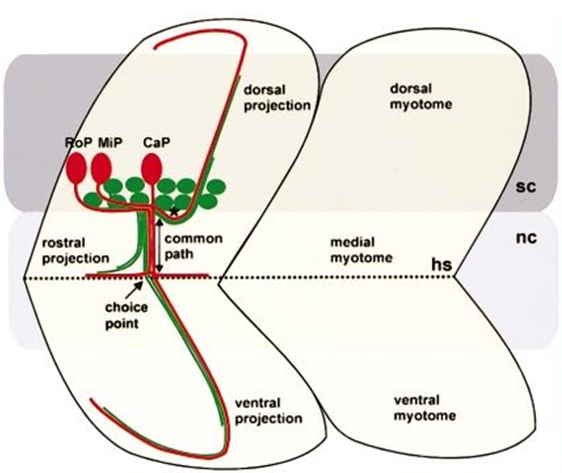
* 그림 출처: Dev Biol. 2001 Jul 1;235(1):86-97.
◆ 2차 운동신경세포 (Secondary motor neuron, SMNs)
- PMN 발달 이후 형성되나 PMN보다 아랫쪽 척수에 훨씬 많은 숫자로 형성됨
- 상대적으로 작은 세포체와 얇은 운동신경을 가지고 있음
- fast, slow muscle 에 운동신경(motor nerve)이 연결됨
- 체절별 근육의 정교한 조절을 담당하여 운동의 미세조율, 유영 지속에 관여
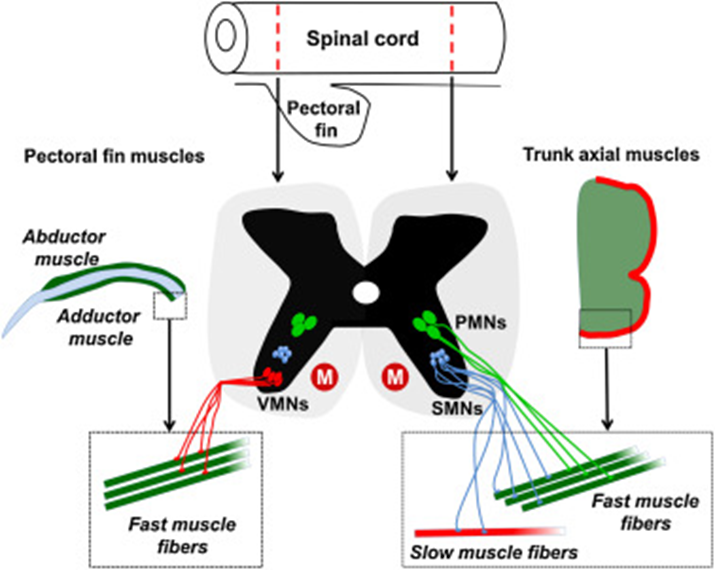
* 그림 출처: Prog Neurobiol. 2014 Jul;118:36-58.
◆ 운동신경 표지 형질전환 제브라피쉬
• mnx1 (previous name- hb9) 유전자 활용 – ex) Tg(mnx1:EGFP), Tg(mnx1:mCherry)
• olig2 유전자 활용 – ex) Tg(olig2:EGFP), Tg(olig2:dsRed)
• Isl1 유전자 활용 – ex) Tg(isl1:GFP)
* 그림 출처: Methods Protoc. 2023, 6(6), 116
* 그림 출처: Toxicology and Applied Pharmacology 237(1):29-40
◆ 형질전환 물고기를 이용한 운동신경 손상 측정 지표
• 운동신경 세포 수의 비교
- 형광 현미경/공초점 현미경을 활용하여 척수를 이미징 한 후 특정 체절 (segment) 내의 세포 수 측정
• 축삭 형태 비교
- 전체 축삭 길이 (from soma to axon tip) 측정
- 분지 (branch point)의 수 및 패턴 관찰
- 잘못된 경로로 뻗은 축삭 (pathfinding error) 빈도 정량화
• 근육신경접합부(neuromuscular junction) 정량화
- presynaptic marker, postsynaptic marker의 수/면적 및 겹침 (co-localization) 비율 비교
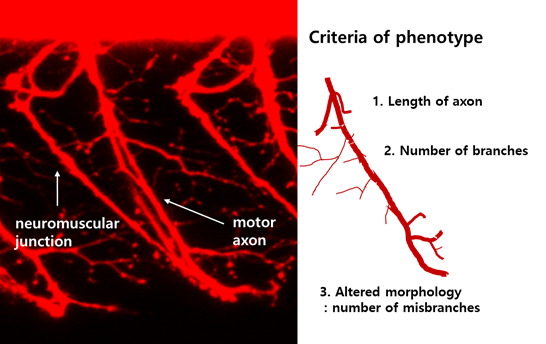
* Tg(olig2:dsRed) 이미징을 통해 측정할 수 있는 운동신경 지표
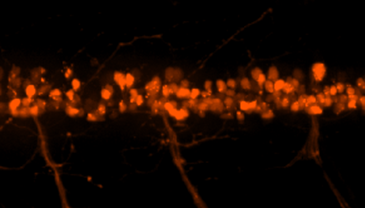
* Tg(mnx1:mCherry) 이미징을 통해 관찰되는 운동신경세포
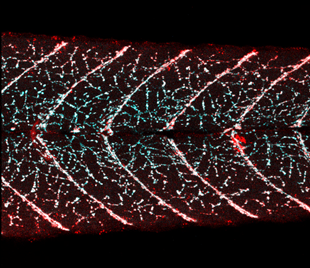
* NMJ colocalization